
DOI:10.1016/j.jcis.2026.140490
全文速览
电催化硝酸盐还原(NO₃RR)是将污染物转化为高值氨的绿色路线,但在中性低浓度条件下,竞争性析氢反应、加氢效率不足和硝酸盐传质缓慢限制了其性能。本研究通过快速焦耳热法将MOFs前驱体转化为三维蜂窝状碳负载的CuNi合金纳米颗粒(Cu₀.₈₁Ni₀.₁₉‑JH)。Cu与Ni的协同效应使催化剂在‑0.75 V(vs. RHE)下氨产率高达5.24 mg h⁻¹ cm⁻²,法拉第效率86.90%。原位红外光谱和实验证明:Cu位点负责NO₃⁻的吸附与活化,Ni位点持续提供*H参与加氢。该电极处理模拟硝酸盐废水,12.5 h去除率99.54%;在Cl⁻/SO₄²⁻共存体系中,N₂选择性始终>99%。组装的Zn‑NO₃电池功率密度达3.90 mW cm⁻²,展示了污染物去除、氨合成与发电的多功能应用前景。
背景介绍
硝酸盐污染是地表水和地下水的主要污染物之一,破坏全球氮循环,引发富营养化等环境问题。NO₃RR可将废弃污染物转化为高值化学品,同时氨作为无碳能源载体(17.5 wt.% H₂)具有广阔前景。然而,NO₃RR涉及9质子‑8电子转移,反应动力学复杂。在中性低浓度硝酸盐废水中,竞争性析氢反应(HER)和中间体加氢不足严重制约了氨的选择性和产率。
铜基材料因与NO₃⁻的LUMO π轨道能级匹配,具有优异的NO₃⁻吸附和活化能力,但加氢能力有限,易积累NO₂⁻。镍基材料可高效解离水产生H,提供加氢所需活性氢。因此,构建CuNi双金属协同催化位点有望实现“吸附‑活化‑加氢”串联催化。此外,MOFs衍生的多孔碳材料兼具高比表面积和导电性,但传统热解易导致结构塌陷。快速焦耳热技术可在秒级内升至超高温并快速冷却,保留MOFs骨架并形成均匀合金。基于此,本研究设计了MOFs衍生的蜂窝碳负载CuNi合金,用于高效NO₃RR。
本文亮点
(1)快速焦耳热构筑蜂窝碳负载CuNi合金:MOFs前驱体经1000℃、80 s焦耳热处理,形成三维蜂窝状多孔碳骨架,CuNi合金纳米颗粒均匀嵌入,比表面积由22.85增至72.12 m²/g,避免结构塌陷。
(2)CuNi协同催化机制:Cu位点吸附活化NO₃⁻,Ni位点高效解离水产生*H,二者串联促进NO₃⁻→NO₂⁻→NO→NH₃快速转化。DFT结合实验表明,电子从Cu转移至Ni,优化了中间体吸附能。
(3)卓越NO₃RR性能:中性低浓度(500 mg‑NO₃⁻/L)下,氨产率5.24 mg h⁻¹ cm⁻²,FE 86.90%,NH₄⁺选择性81.4%。12.5 h硝酸盐去除率99.54%,30 h后仅余2.19 mg‑NO₂⁻/L。
(4)多功能应用:Cl⁻/SO₄²⁻共存体系中N₂选择性>99%;组装Zn‑NO₃电池开路电压1.48 V,功率密度3.90 mW cm⁻²,兼具发电、脱氮、产氨功能。
图文解析
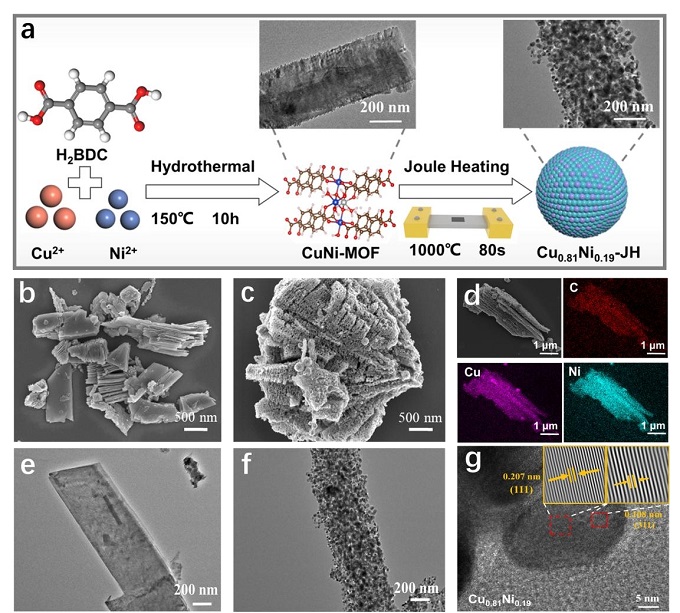
图1:材料合成与形貌表征
(a) Cu₀.₈₁Ni₀.₁₉‑JH的制备示意图。(b) CuNi‑MOF的SEM图像。(c) Cu₀.₈₁Ni₀.₁₉‑JH的SEM图像。(d) Cu₀.₈₁Ni₀.₁₉‑JH的EDS元素分布图。(e) CuNi‑MOF的TEM图像。(f‑g) Cu₀.₈₁Ni₀.₁₉‑JH的TEM图像。
图1a展示水热合成CuNi‑MOF(片层堆叠结构,图1b),随后经焦耳热(1000℃, 80 s, Ar)转化为三维蜂窝状多孔碳(图1c),均匀负载CuNi合金纳米颗粒。EDS(图1d)显示Cu、Ni、C均匀分布。TEM(图1e‑g)证实MOF的准矩形形貌在焦耳热后得以保留,合金纳米粒子嵌入碳骨架,HRTEM晶格条纹0.207 nm对应Cu₀.₈₁Ni₀.₁₉的(111)/(311)晶面。
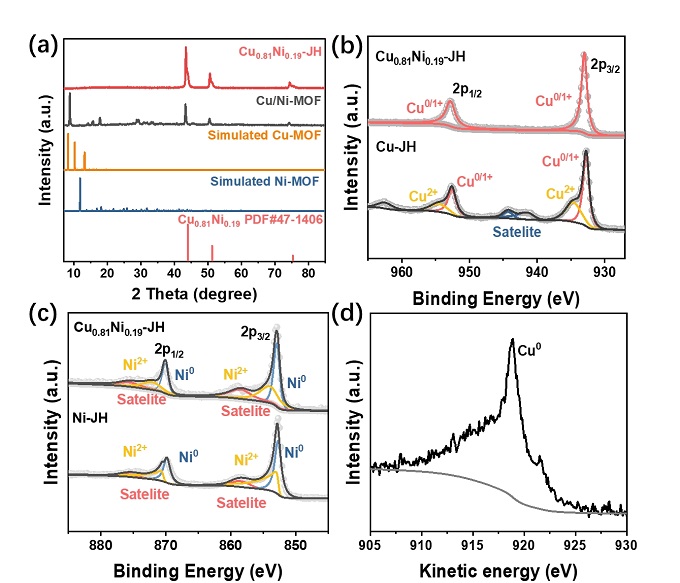
图2:材料物相与表面化学态
(a) CuNi‑MOF和Cu₀.₈₁Ni₀.₁₉‑JH的XRD谱图。(b) Cu 2p XPS谱图。(c) Ni 2p XPS谱图。(d) Cu LMM俄歇谱图。
XRD图谱显示CuNi‑MOF的衍射峰相对于模拟Cu‑MOF向高角度偏移,证实Ni部分取代Cu。焦耳热处理后,产物在43.60°、50.79°、74.68°出现Cu₀.₈₁Ni₀.₁₉合金相(PDF#47‑1406)的特征峰。XPS高分辨谱中,Ni 2p的Ni⁰结合能负移0.20 eV,Cu 2p的Cu⁰/¹⁺正移0.32 eV,表明电子从Cu转移至Ni,优化了电子结构。Cu LMM(图2d)确认Cu主要以零价态存在。
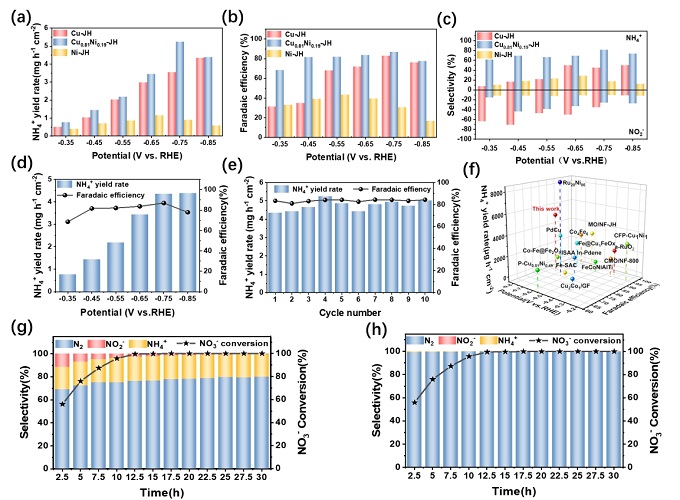
图3:电催化NO3RR性能
(a) Cu‑JH、Cu₀.₈₁Ni₀.₁₉‑JH和Ni‑JH在不同电位下的氨产率;(b) 对应的法拉第效率;(c) NH₄⁺选择性;(d) 不同电位下的氨产率与法拉第效率;(e) 10次循环稳定性测试;(f) 与已报道催化剂的性能对比;(g) 模拟废水中硝酸盐去除率及产物选择性;(h) Cl⁻/SO₄²⁻共电解质中的硝酸盐去除率与N₂选择性。
Cu₀.₈₁Ni₀.₁₉‑JH在‑0.75 V下氨产率5.24 mg h⁻¹ cm⁻²,FE 86.90%(图3a,b),NH₄⁺选择性81.4%,10次循环后性能稳定。图3g显示,处理模拟废水12.5 h后NO₃⁻去除率99.54%,主要产物为N₂(76.29%)和NH₄⁺(21.24%)。在Cl⁻/SO₄²⁻共存体系中(图3h),N₂选择性始终>99%,30 h去除率98.87%,归因于活性氯的断点氯化作用。
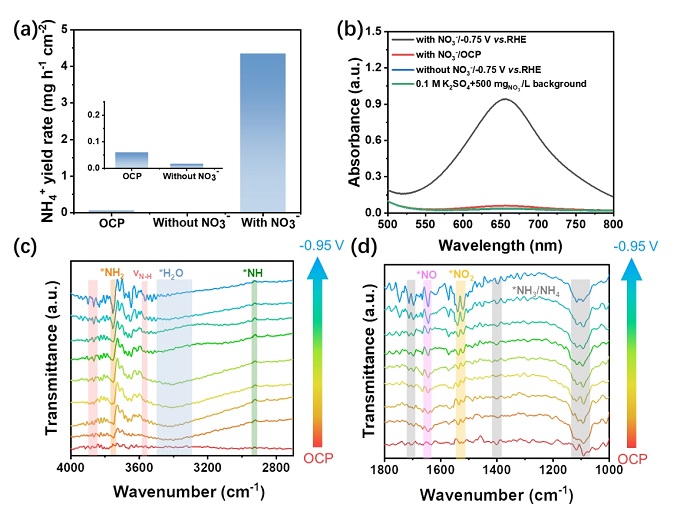
图4:反应机理原位红外与活性氢验证
(a) 有无硝酸盐时Cu₀.₈₁Ni₀.₁₉‑JH的NH₄⁺产率对比;(b) 不同条件下的UV‑vis光谱;(c,d) Cu₀.₈₁Ni₀.₁₉‑JH在NO₃RR过程中的原位FTIR光谱。
对照实验证实氨产物来源于硝酸盐还原。原位FTIR显示在1660 cm⁻¹(NO₂)、1524 cm⁻¹(NO)、3750 cm⁻¹(NH₂)、2957 cm⁻¹(NH)和1420/1710 cm⁻¹(NH₃)等处检测到关键中间体,且峰强随电位负移增强,表明Cu₀.₈₁Ni₀.₁₉‑JH表面发生连续的脱氧加氢反应。活性氢淬灭实验显示加入TBA后Ni‑JH的FE从31%骤降至11%,而Cu‑JH仅从72%降至69%,证实Ni位点是*H的主要供应源。
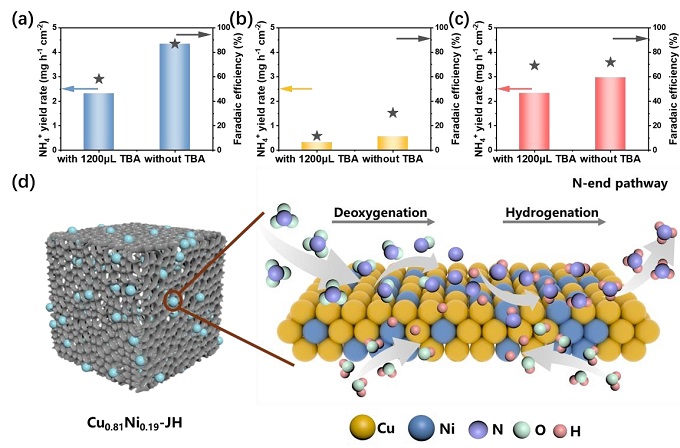
图5:CuNi协同催化机制示意图
(a) Cu₀.₈₁Ni₀.₁₉‑JH、(b) Ni‑JH和(c) Cu‑JH在添加TBA前后的氨产率和法拉第效率;(d) 反应机理示意图。
图5a‑c定量显示TBA加入后,Ni‑JH的FE下降最显著,Cu‑JH变化最小,进一步证明Ni位点负责*H生成。图5d总结了反应路径:Cu位点吸附活化NO₃⁻并将其还原为NO₂⁻/NO,Ni位点提供*H,逐步加氢生成NH₃(NO₃⁻ → NO₂⁻ → NO → NH₂ → NH₃ → NH₄⁺)。
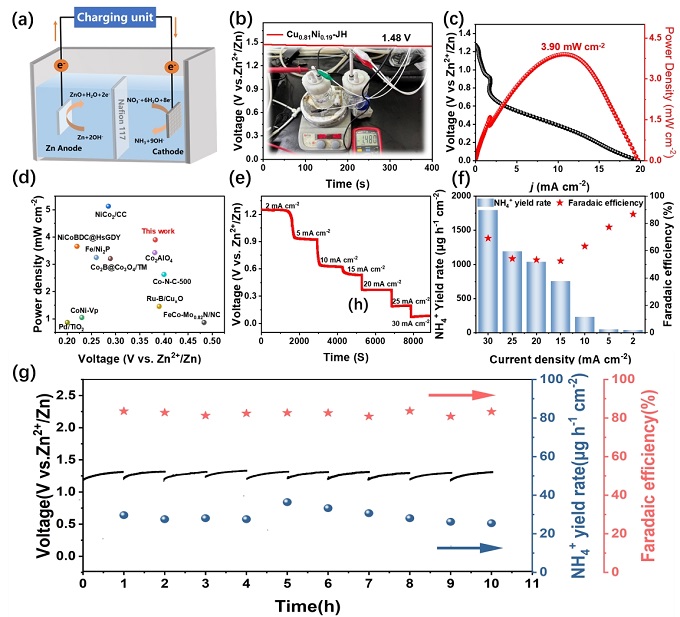
图6:以Cu₀.₈₁Ni₀.₁₉‑JH为阴极的Zn‑NO₃电池的电化学性能
(a) Zn‑NO₃电池示意图;(b) 开路电压;(c) 放电曲线与功率密度;(d) 与已报道Zn‑NO₃电池的功率密度和电压对比;(e) 不同电流密度下的放电电压;(f) 不同电流密度下的氨产率与法拉第效率;(g) 2 mA cm⁻²下的长期稳定性测试。
组装的Zn‑NO₃电池开路电压1.48 V,最大功率密度3.90 mW cm⁻²,优于多数文献报道(图6d)。在不同电流密度下放电平台稳定。图6f显示氨产率随电流密度增加而上升,FE在2 mA cm⁻²时达87%。图6g表明在2 mA cm⁻²下连续运行,放电电压、氨产率和FE均无明显衰减,展示出良好的实际应用潜力。
总结与展望
本研究利用快速焦耳热技术成功制备了MOFs衍生的蜂窝碳负载CuNi合金催化剂(Cu₀.₈₁Ni₀.₁₉‑JH)。该方法在秒级内完成高温热解与快速冷却,保留了MOFs的三维多孔结构,形成了均匀的CuNi合金纳米颗粒。Cu与Ni的电子协同效应使催化剂在中性低浓度硝酸盐废水中实现了高效、高选择性的NO₃RR:氨产率5.24 mg h⁻¹ cm⁻²,FE 86.90%,且稳定性优异。原位光谱和活性氢淬灭实验阐明了Cu位点吸附活化NO₃⁻、Ni位点提供*H的串联催化机制。此外,催化剂在含Cl⁻废水中表现出>99%的N₂选择性,避免了二次污染;组装的Zn‑NO₃电池同时实现了发电、脱氮和产氨三功能。
该工作为MOFs衍生催化剂的设计提供了新思路:快速焦耳热技术可推广至其他双金属体系,用于能源与环境催化。未来可进一步优化合金比例和碳孔结构,提升低浓度硝酸盐下的反应动力学,并探索其在真实工业废水处理中的规模化应用。
本文使用的焦耳加热装置由合肥原位科技有限公司研发,感谢老师支持和认可!
